新闻动态
回顾2025 年,烈冰生物在单细胞与多组学服务领域继续稳步推进各项科研项目,凭借成熟的单细胞多组学实验体系和不断优化的分析平台,我们在科研服务中取得了丰硕成果,助力发表文献井喷式增长,持续保持领先的技术领域优势。
一、助力发表文献整体概况
2025 年,烈冰生物围绕单细胞及多组学研究,协助科研团队完成了一系列高质量科研成果发表:
发表单细胞领域论文总数:100+(不完全统计)
累计影响因子:1310.3
高分论文(IF ≥10):63篇
上述成果覆盖肿瘤免疫、衰老机制、发育生物学、免疫调控及多组学整合等多个前沿研究方向,彰显烈冰生物在高难度科研项目中的持续交付能力以及在大规模科研发表支持中的稳定性与可靠性。
二、全流程的服务体系
高质量科研发表并非单一实验或分析环节的结果,而是建立在体系化、标准化服务流程之上。烈冰生物构建了覆盖科研全流程的单细胞多组学服务体系:
样本处理阶段:自研组织解离仪,针对不同样本类型均可温和高效解离组织样本,获得高质量的细胞悬液。
细胞质检捕获阶段:自研质检仪器Novel BrilliantTM可快速精准获得细胞悬液质检结果;进口10x Genomics、BD Rhapsody单细胞捕获平台结合自研单细胞捕获平台NovelCyto®、NovelDrop®适配不同样本类型,提供灵活高效的单细胞捕获方案。
实验交付阶段:自研单细胞建库工作站,全自动建库,最大程度避免人工误差,高效稳定交付高质量原始数据。
数据分析与发表支持阶段:自研数据分析平台,支持数据质控、标准化流程构建、多批次数据一致性校验;科研发表的数据分析、结果解读与高质量可视化图表输出。
三、自研单细胞平台赋能科研
烈冰持续投入自研能力建设,自主开发单细胞捕获平台NovelCyto®与单细胞数据分析平台CytoNavigator®为科研团队队提供更加灵活、高效的单细胞服务和支持。
烈冰单细胞捕获平台NovelCyto®在产出的数据质量上具备比肩国际微孔法平台,具备高效、高质量、高性价比的特点,让前沿技术惠及更多科研团队,加速单细胞技术的国产化进程。
2025 年,烈冰自研单细胞捕获平台NovelCyto® 在科研实践中已初露锋芒,部分助力研究成果已经成功发表:
烈冰自研单细胞数据分析平台CytoNavigator®,拥有简单易用的一键分析页面、高可交互的单细胞可视化系统、自组织的结果简报,结果全流程可追溯,全程零代码的特点,一直是科研团队必备的分析工具。
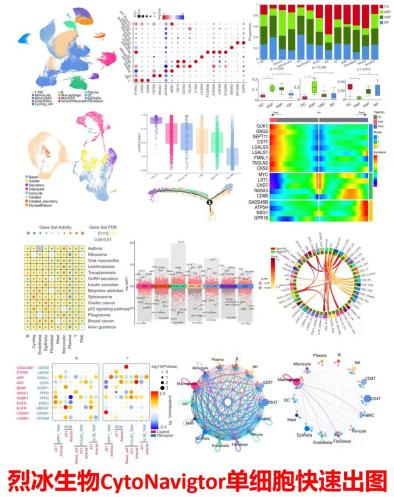
2025年CytoNavigator®数据分析平台助力科研团队产出了大量高质量文章:
1、单细胞多组学图谱揭示成人与儿童脓毒症的解剖特异性免疫特征(《Nature Immunology》 IF=27.6)
2、成人前列腺的空间解析转录组学分析(《Nature Genetics》 IF=29.0)
3、单细胞多组学图谱揭示成人与儿童脓毒症的解剖特异性免疫特征(《Immunity》 IF=26.3)
值得一提的是,我们在盘点助力文献的过程中还发现一篇有趣的文献:
中文标题:促肾上腺皮质激素释放激素从梨状皮层到杏仁核的信号传导介导阿片类药物成瘾中的社会同质性
科研团队基于烈冰CytoNavigator®数据分析云平台,自主挖掘公开数据库数据并完成分析与发表,文献发表于《Neuron》(IF=15),体现了数据分析云平台在科研赋能与技术开放性方面的价值。
烈冰不仅提供实验与分析服务,更能通过自研数据分析平台,帮助科研人员独立发现并验证具有发表潜力的科研结论。
四、高影响力论文发表案例
高影响力期刊发表的科研成果,往往对实验稳定性、数据质量及分析深度提出更高要求。
2025 年,烈冰在多项复杂单细胞与多组学研究中,持续参与并支撑科研团队完成高标准的数据交付与分析工作。
以下选取部分具有代表性的研究成果,展现单细胞与多组学技术在解析复杂生物学问题中的研究意义。
1、
发表期刊:Cancer Cell
影响因子:IF=44.5
研究意义:
该研究首次揭示了KMT2C(一种组蛋白H3K4甲基转移酶)缺失在去势抵抗性前列腺癌(CRPC)中驱动腺癌向双阴性前列腺癌(DNPC)转分化的关键机制,阐明了DNPC并非源于基底细胞转化,而是由管腔细胞在雄激素剥夺疗法(ADT)压力下经ΔNp63依赖途径转分化而来,并通过激活脂肪酸合成及HRAS棕榈酰化-MAPK信号轴维持生长和耐药性。
这不仅为理解前列腺癌谱系可塑性及耐药提供了全新理论框架,更通过靶向脂肪酸合成抑制剂TVB-2640展现出治疗DNPC的转化潜力,为临床克服AR靶向治疗耐药提供了新的策略方向。
2、
发表期刊:Nature Nanotechnology
影响因子:IF=34.9
研究意义:
该研究首次成功构建并验证了一个可编程、具有细胞靶向性的病毒样颗粒(VLP)系统,用于在活体动物体内递送CRISPR-Cas9核糖核蛋白(RNP)。这一系统不仅实现了在复杂生物环境中(如眼睛和大脑)对特定细胞类型(如视网膜色素上皮细胞、神经元)的高效、精准基因编辑,更在两个截然不同的重大疾病模型(血管性疾病和神经退行性疾病)中同时展现出治疗效力,并将安全性和有效性验证推进至非人灵长类及患者来源的神经元水平,为开发下一代“即用型”、安全可控的体内基因编辑疗法铺平了道路。
3、
发表期刊:Cell
影响因子:IF=42.5
研究意义:
该研究是全球首个抗 BCMA CAR-T 治疗 PMS 的人体试验(NCT04561557),5 例患者(1 例原发性 PMS、4 例继发性 PMS)接受治疗后,展现出三大关键疗效与安全性特征:
1.安全性优异:仅出现 1 级细胞因子释放综合征(CRS),无≥2 级 CRS;≥3 级血细胞减少均在 40 天内恢复,无严重贫血或血小板减少。
2.中枢靶向性强:CAR-T 细胞可穿透血脑屏障,在脑脊液中持续扩增且耗竭特征降低,同时实现中枢(脑脊液、骨髓)与外周的浆细胞深度清除。
3.神经功能显著改善:所有患者 EDSS 评分(残疾评估量表)下降,9 孔插板试验(上肢功能)、25 英尺步行试验(下肢功能)耗时缩短,脑脊液神经丝轻链(NfL,神经损伤标志物)水平降低,且无新增脑病灶。
4、
发表期刊:Signal Transduction and Targeted Therapy
影响因子:IF=52.7
研究意义:
该研究首次在大规模前瞻性研究中证实了帕博利珠单抗联合放化疗(PPCT)作为局部晚期可切除食管鳞癌(ESCC)新辅助治疗的安全性与可行性,并揭示了其潜在疗效。研究不仅提供了关键的临床数据,更重要的是通过单细胞测序和动物模型首次发现:基线血清IL-6水平可作为预测PPCT疗效的潜在生物标志物,而中和IL-6能显著增强CD4⁺ T细胞的细胞毒性,从而与抗PD-1疗法产生协同抗肿瘤效应。 这一发现不仅为理解免疫联合治疗的耐药机制提供了新视角,更为未来优化ESCC的免疫治疗策略(如联合IL-6阻断)开辟了全新的转化方向。
5、
发表期刊:Signal Transduction and Targeted Therapy
影响因子:IF=33
研究意义:
该研究首次系统揭示了化疗相关性脂肪性肝炎(CASH)在结直肠癌肝转移患者中引发高复发率的免疫机制,通过单细胞转录组分析发现CASH肝脏微环境中特异性富集具有免疫抑制功能的MARCO⁺巨噬细胞,并伴随CD8⁺ TOX⁺ T细胞耗竭和DNAJB1⁺ NK细胞应激活化,这些细胞共同构成一个以MARCO⁺巨噬细胞为核心的免疫抑制网络,直接促进肿瘤肝转移和复发;研究进一步在动物模型中证实敲除MARCO可显著抑制肝转移并逆转T细胞耗竭,为理解CASH不良预后的免疫基础提供了新视角,也为针对MARCO⁺巨噬细胞及其相关免疫网络的靶向治疗提供了潜在策略,有望改善化疗副作用并提升肝转移患者的免疫治疗效果。
五、总结与展望
通过体系化实验流程、自研分析平台与面向发表的服务理念,烈冰生物在 2025 年持续为科研团队提供可靠、高质量的科研发表支持,帮助研究人员将精力集中于科学问题本身。
2026 年,烈冰将进一步优化单细胞与多组学服务流程,持续提升平台能力与分析深度,为更多高难度科研项目提供坚实支撑,助力更多科研成果顺利发表。
如有单细胞多组学合作需求,欢迎后台留言咨询。
