口腔白斑病(oral leukoplakia,OL)是最重要的口腔潜在恶性疾患之一,上皮异常增生是其病理学特征,且因口腔部位相对表浅易于观测,可作为全身癌前病变的代表性疾病,是癌前病变发生发展的良好研究模型。但现阶段的药物治疗、手术、激光、冷冻、光动力等疗法均不能有效降低口腔白斑病的癌变率,并且口腔白斑病还存在易复发、多发、多次癌变等临床困境。因此,针对口腔白斑病研发具有抑制和逆转作用的全身用药,特别是对于口腔黏膜具有区域化癌变潜能的患者,具有重要的临床意义和社会价值。

上海交通大学医学院附属第九人民医院口腔黏膜病科副主任医师施琳俊,上海交通大学基础医学院生化细胞系硕士生杨于权,博士生李梦莹为该论文的共同第一作者;上海交通大学基础医学院的贾浩副研究员,侯照远研究员及医学院附属第九人民医院口腔黏膜病科沈雪敏主任医师为该论文的共同通讯作者。该文章发表在Molecular Therapy杂志(IF=11.454)上,题目为“LncRNA IFITM4P promotes immune escape by up-regulating PD-L1 via dual mechanism in oral carcinogenesis”。
烈冰生物参与了本研究中的转录组测序和部分数据分析工作,本期文献分享,我们也有幸邀请了文章的作者施琳俊副主任医师从第一视角为大家进行详细的文章解析,下面跟随我们的步伐一起看看文章的研究思路和成果吧~
技术手段
lncRNA+转录组测序,qRT-PCR免疫组化(mIHC),免疫共沉淀(co-IP)
RNA免疫沉淀(RIP),染色质免疫共沉淀(CHIP),Western Blot等
实验分组
正常黏膜(NM) 、口腔白斑病( OL )和口腔鳞状细胞癌(OSCC)组织样本
研究结果
01 IFITM4P与口腔白斑病程进展高度相关
通过高通量筛选,作者发现相较于正常组织样本(NM),lncRNA IFITM4P在口腔黏膜白斑病/鳞癌组织(OL/OSCC)中存在高表达,且随着病程的进展其表达水平也在逐渐升高,该结果也与qRT-PCR、RNA scope等实验的验证结果相一致。
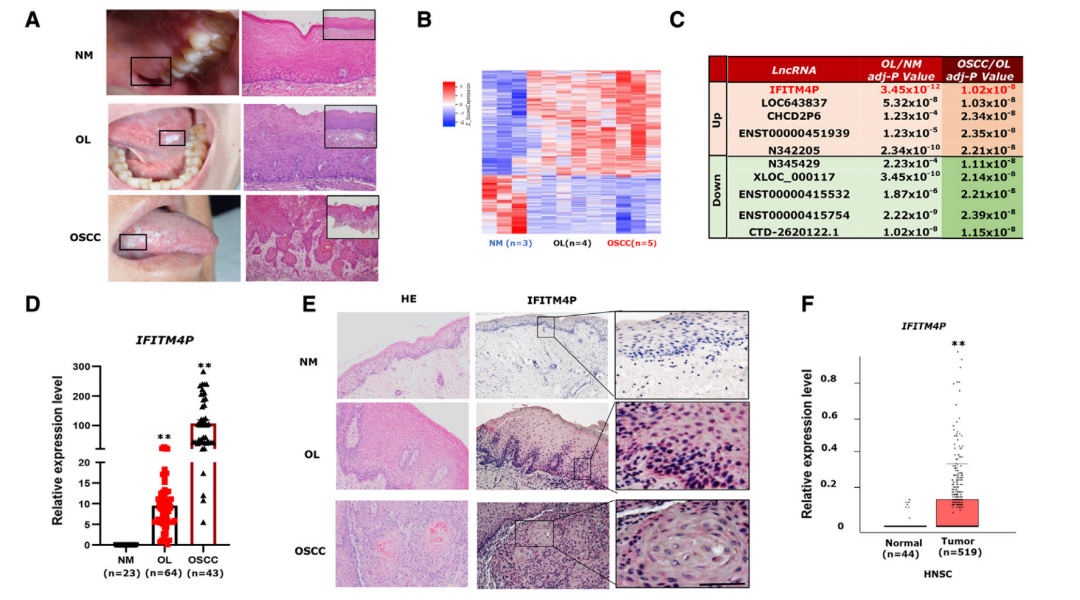
02 IFITM4P可作为口腔白斑病恶变的指标
为确定IFITM4P在口腔癌变过程中的作用,研究者利用慢病毒载体转染口腔白斑细胞系Leuk-1和口腔鳞癌细胞系HN4,结果发现外源IFITM4P可显著促进这两种细胞的增殖,动物实验验证发现,相较于对照组,IFITM4P过表达促进了口腔鳞癌的发展,这表明IFITM4P可作为诊断口腔黏膜白斑恶变的指标。
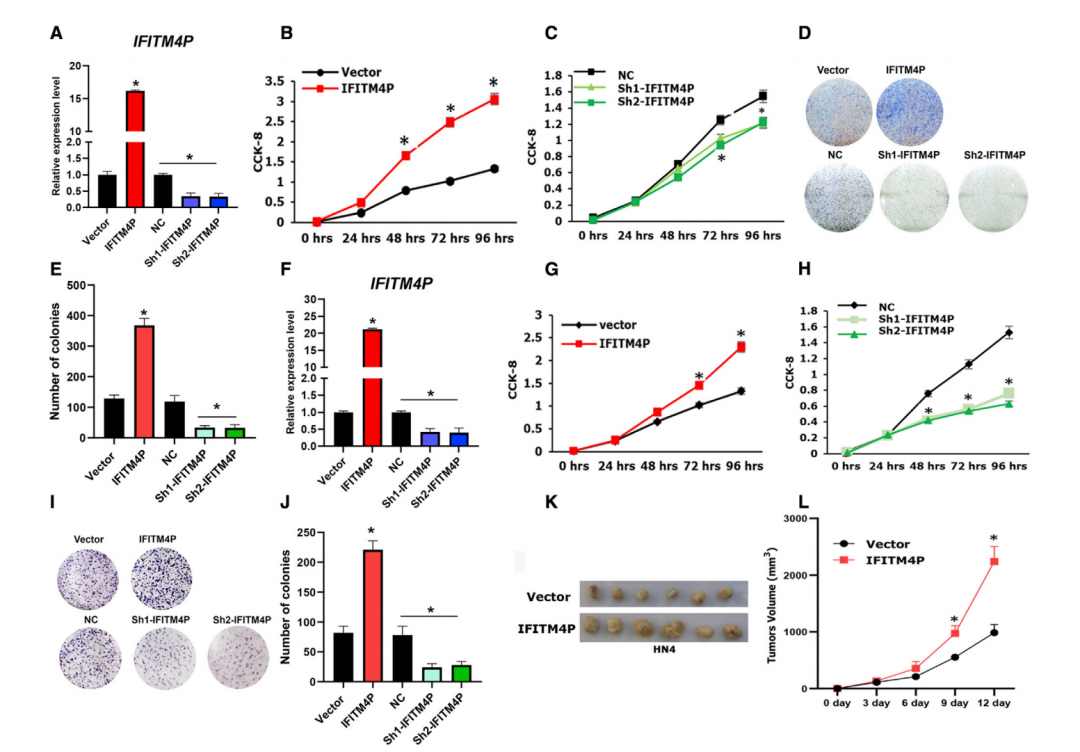
03 PD-1抗体抑制疾病恶性进展
进一步,作者利用高通量筛选,发现PD-L1的表达水平随着恶变程度的增加而升高。此外,作者在实验中首次构建了LPS(脂多糖)联合4NQO诱导的“炎症-口腔白斑小鼠模型”,动物实验证实炎症刺激可以加速舌白斑小鼠模型恶性进展。通过给患病小鼠注射PD-1抗体后,发现PD-1抗体可以显著阻断口腔白斑恶性进展,且在炎症诱发的小鼠白斑恶性进展模型中的抑制效果更好。
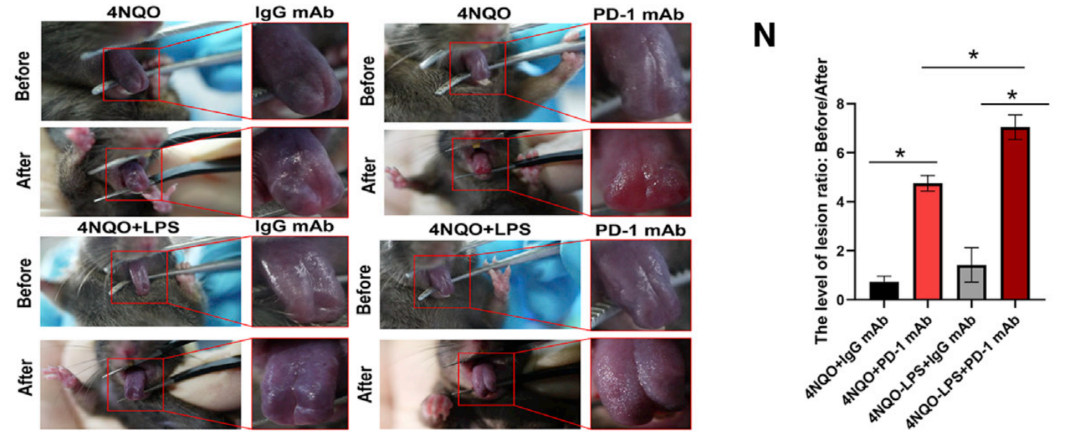
04 口腔黏膜白斑病免疫逃逸机制
在机制分析层面,作者发现相较于正常组织,IFITM4P受LPS刺激后可以进行核质穿梭,具体来说:在细胞质内,IFITM4P与SASH1形成复合体,通过磷酸化激活了TAK1-NF-κB途径,NF-κB的入核促进了PD-L1的表达。此外,LPS也可以促进IFITM4P的进入细胞核,在核内进一步招募去甲基化酶KDM5A并抑制了PTEN的表达,进而削弱了PTEN对PD-L1的抑制作用,升高了PD-L1的表达水平。IFITM4P通过胞质和胞核两种机制协同促进了口腔白斑/鳞癌细胞中PD-L1的表达,促使口腔黏膜白斑病发生免疫逃逸。
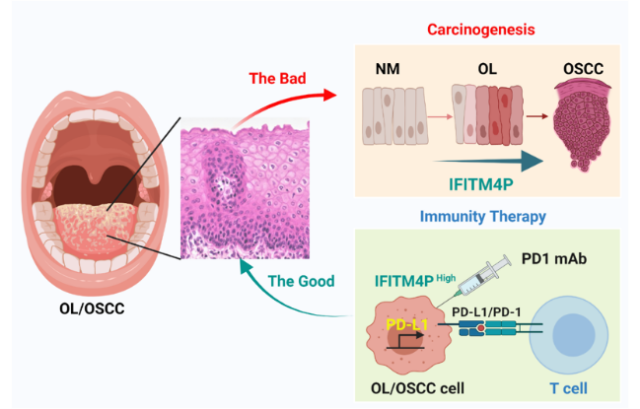
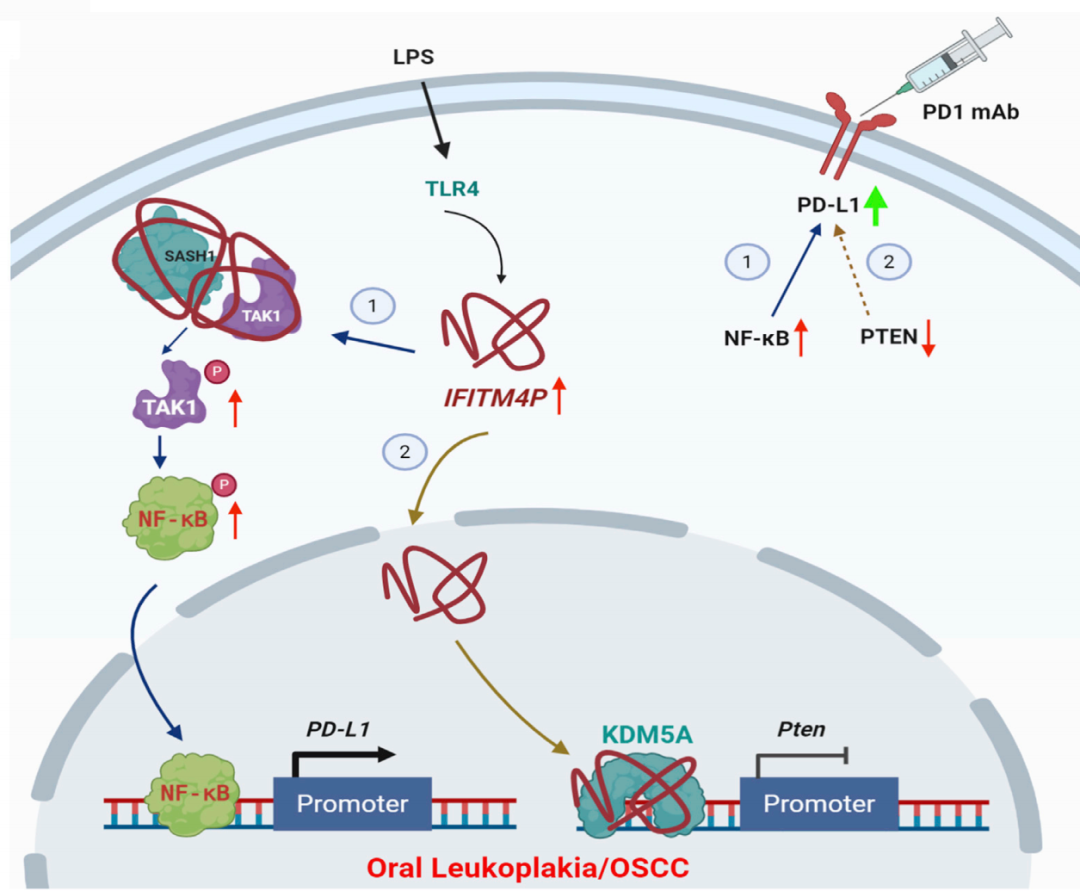
文章总结
研究人员利用口腔白斑病组织和口腔鳞癌组织样本通过高通量筛选的方法,分析发现了IFITM4P和PD-L1的表达水平随着组织恶性程度的增加而升高,IFITM4P可作为早期诊断口腔黏膜白斑病恶变的指标。同时研究团队利用动物模型也发现了IFITM4P高表达的荷瘤小鼠对PD-1单抗的响应更好,可考虑将PD-1单抗作为治疗高表达IFITM4P口腔黏膜白斑的有效治疗手段。
原文链接
https://doi.org/10.1016/j.ymthe.2022.01.003