本期,小编带大家来看看2月份有哪些单细胞转录组测序相关的高分文章吧~
2月份共整理21篇高分文献(IF>20),其中,构建单细胞图谱的文章有6篇,涉及首份人类胸腺细胞图谱,灵长类动物衰老卵巢细胞图谱、以及对小鼠肠道、皮肤、视交叉上核和内皮细胞的单细胞转录组图谱进行绘制。生长发育有6篇,包括干细胞分化、类原肠胚、类器官;肿瘤相关的文献3篇,免疫相关的文献4篇;神经科学2篇。
(扫描文末二维码,获取所有文章连接~)
下面小编将针对7篇CNS文献进行简单介绍:
一、

题目:MAFG-driven astrocytes promote CNS inflammation
DOI号:10.1038/s41586-020-1999-0
发表期刊:Nature
影响因子:43.07
发表日期:20200212
研究方向:多发性硬化症
摘要:多发性硬化症是中枢神经系统的慢性炎性疾病。星形胶质细胞可引起多发性硬化症发病,但对星形胶质细胞的异质性及其调控知之甚少。研究人员通过单细胞RNA测序结合细胞特异性Ribotag RNA谱分析、转座酶可及染色质测序分析(ATAC–seq)、染色质免疫沉淀测序(ChIP-seq)、DNA甲基化的全基因组分析以及基于CRISPR-Cas9的体内遗传干扰技术,报道了多发性硬化中的星形胶质细胞及其临床前模型实验性自身免疫性脑脊髓炎(EAE)的分析结果。并且在EAE和多发性硬化症中鉴定出星形胶质细胞,其特征在于NRF2的表达减少和MAFG的表达增加,而MAFG与MAT2α协同作用以促进DNA甲基化并抑制抗氧化剂和抗炎转录程序。星形胶质细胞中的粒细胞-巨噬细胞集落刺激因子(GM-CSF)信号驱动MAFG和MAT2α的表达以及促炎性转录模块,导致EAE中枢神经系统病理,并可能导致多发性硬化。因此,这些结果确定了多发性硬化症的候选治疗靶标。
二、

题目:Single-cell and spatial transcriptomics reveal somitogenesis in gastruloids
DOI号:10.1038/s41586-020-2024-3
发表期刊:Nature
影响因子:43.07
发表日期:20200219
研究方向: 发育-类原肠胚
摘要:类原肠胚是胚胎干细胞的三维聚集体,在着床后表现出哺乳动物发育的关键特征,包括胚层分化和轴向形成。目前,人们已经利用显微镜研究了类原肠胚中少数基因的表达模式,并且尚不清楚在类原肠胚在模拟胚胎时全基因组表达模式到达何种程度。研究人员使用单细胞RNA测序和空间转录组学来比较了小鼠类原肠胚与小鼠胚胎。他们确定了各种以前未知的类原肠胚细胞类型,并表明在胚胎和类原肠胚之间相似地表达了体节发生的关键调控因子。使用实时成像,研究人员表明体节发生时钟活跃在类原肠胚中,并具有类似于体内的动态。因为类原肠胚可以大量生长,所以他们进行了一个小型筛选,从而揭示了降低的FGF信号如何诱导胚胎中的短尾表型。最后,研究人员证明了在基质胶中包埋会诱导类原肠胚产生具有正确头尾模式的体节,随着时间沿前后方向依次出现。因此,这项研究显示了类原肠胚作为模型系统的能力,其能够以高通量方式研究体外发育和体节发生。
三、

题目:Peripheral T cell expansion predicts tumour infiltration and clinical response
DOI号:10.1038/s41586-020-2056-8
发表期刊:Nature
影响因子:43.07
发表日期:20200226
研究方向:肿瘤-免疫T细胞
摘要:尽管阻断PD 1及其配体PDL 1相互作用的抗体在癌症治疗中取得了巨大的临床成功,但其涉及的机制仍然未知。在肿瘤免疫中阐述T细胞起源和命运的主要限制因素是缺乏癌症患者中T细胞个体克隆型分布的定量信息。通过对患有不同类型癌症的患者进行RNA和T细胞受体深层单细胞测序,研究人员揭示了肿瘤、正常邻近组织和外周血中各种T细胞和T细胞受体的分布。足够的证据表明不仅在肿瘤内而且在正常的相邻组织中,效应样T细胞均呈克隆型扩增。具有这种克隆型扩增基因标记的患者对抗PDL1治疗的反应最佳。值得注意的是,在外周血中还可以检测到在肿瘤和正常相邻组织中发现的这种克隆型扩增,这提供了一种方便的患者识别方法。对该数据以及其它几个外部数据集的分析表明,来自肿瘤外部新鲜的、无穷尽的替代细胞补充了肿瘤内T细胞(尤其是反应性患者),这表明这些患者的癌症免疫周期持续激活并可能与临床反应有关。
四、

题目:A cell atlas of human thymic development defines T cell repertoire formation
DOI号:10.1126/science.aay3224
发表期刊:Science
影响因子:41.04
发表日期:20200221
研究方向:图谱-胸腺T细胞
摘要:胸腺为T细胞的发育分化提供了一个良好的环境,这一过程是由它们与多种胸腺细胞类型的相互作用所协调的。研究人员使用单细胞RNA测序来创建人类胸腺的细胞图谱,并重建T细胞分化轨迹和T细胞受体(TCR)重组动力学。利用这种方法,研究人员识别并定位了原位CD8αα+T细胞群、胸腺成纤维细胞亚型和活化的树突状细胞状态。此外还揭示了TCR重组和选择的偏差,这是由于基因组位置和谱系承诺的动力学。综上所述,这些数据提供了一个完整的人类胸腺图谱,对人类T细胞的发育进行了高分辨率的普查。
五、

题目:Lymphoma Driver Mutations in the Pathogenic Evolution of an Iconic Human Autoantibody
DOI号:10.1016/j.cell.2020.01.029
发表期刊:Cell
影响因子:36.22
发表日期:20200213
研究方向:淋巴瘤
摘要:许多自身免疫性疾病中存在致病性自身抗体,但尚不了解它们如何逃避细胞免疫检查点的控制。利用单细胞多组学分析,研究人员发现淋巴样恶性肿瘤与由常见类风湿因子自身抗体引起的混合型冷球蛋白血症的共享机制。通过将单细胞DNA和RNA测序与血清抗体肽测序和抗体合成相结合,研究人员发现产生积累突变的克隆树是由产生致病性自身抗体的罕见循环B淋巴细胞构成的。调控B细胞增殖和V(D)J突变的基因(CARD11,TNFAIP3,CCND3,ID3,BTG2和KLHL6)中存在淋巴瘤引起的突变,这些突变都存在流氓B细胞产生致病性自身抗体过程中。抗体V(D)J突变通过在低温度下使抗原结合的自身抗体发生相变成为不溶性聚集物而赋予其致病性。这些结果揭示了人类淋巴瘤肿瘤形成的前阶段以及造成致病性自身抗体产生的一系列体细胞突变。
六、

题目:Single-Cell Transcriptomic Atlas of Primate Ovarian Aging
DOI号:10.1016/j.cell.2020.01.009
发表期刊:Cell
影响因子:36.22
发表日期:20200206
研究方向:图谱-灵长类动物卵巢
摘要:卵巢衰老和女性与年龄相关的生育力下降的分子机制仍不清楚。研究人员调查了年轻人和老年人的非人类灵长类动物(NHP)卵巢的单细胞转录组情况,并鉴定了七种具有不同基因表达特征的卵巢细胞,包括卵母细胞和六种类型的卵巢体细胞。卵母细胞基因表达动态的深入解剖揭示了在顺序和逐步发展阶段的四个亚型。细胞类型特异性衰老相关转录变化的进一步分析揭示了早期卵母细胞和颗粒细胞特有的抗氧化剂信号传导的紊乱,表明氧化损伤是卵巢功能下降的关键因素。此外,在老年妇女的颗粒细胞中观察到失活的抗氧化途径、活性氧增加和凋亡。这项研究以单细胞分辨率全面了解了灵长类动物卵巢衰老背后的细胞类型特异性机制,揭示了新的诊断性生物标记物以及与年龄相关人类卵巢疾病的潜在治疗靶标。
七、

题目:Single-Cell Transcriptome Atlas of Murine Endothelial Cells
DOI号:10.1016/j.cell.2020.01.015
发表期刊:Cell
影响因子:36.22
发表日期:20200213
研究方向:图谱-小鼠内皮细胞
摘要:人们对不同组织EC的异质性仍然了解不完全。研究人员从小鼠11种组织中构建了32000多个单EC转录组图谱,并鉴定了78个EC亚群,包括健康组织中的Aqp7+肠毛细血管和血管生成EC。来自大脑/睾丸、肝脏/脾脏、小肠/结肠和骨骼肌/心脏的EC成对地表达部分重叠的标记基因。与异质毛细管EC相比,动脉、静脉和淋巴EC在更多的组织中具有更多相同标志物。来自不同血管床(动脉、毛细血管、静脉、淋巴管)的EC表现出跨组织的转录组相似性,但是组织(而非血管)类型导致EC异质性。代谢转录组分析揭示了EC相似的组织分组现象和组织之间以及单个组织内血管床之间的EC的异质代谢基因特征,它们具有组织类型依赖性模式。EC图谱在公共scRNA-seq数据集中鉴定EC亚型,并提供了一个强大的发现工具和一个有价值的资源。
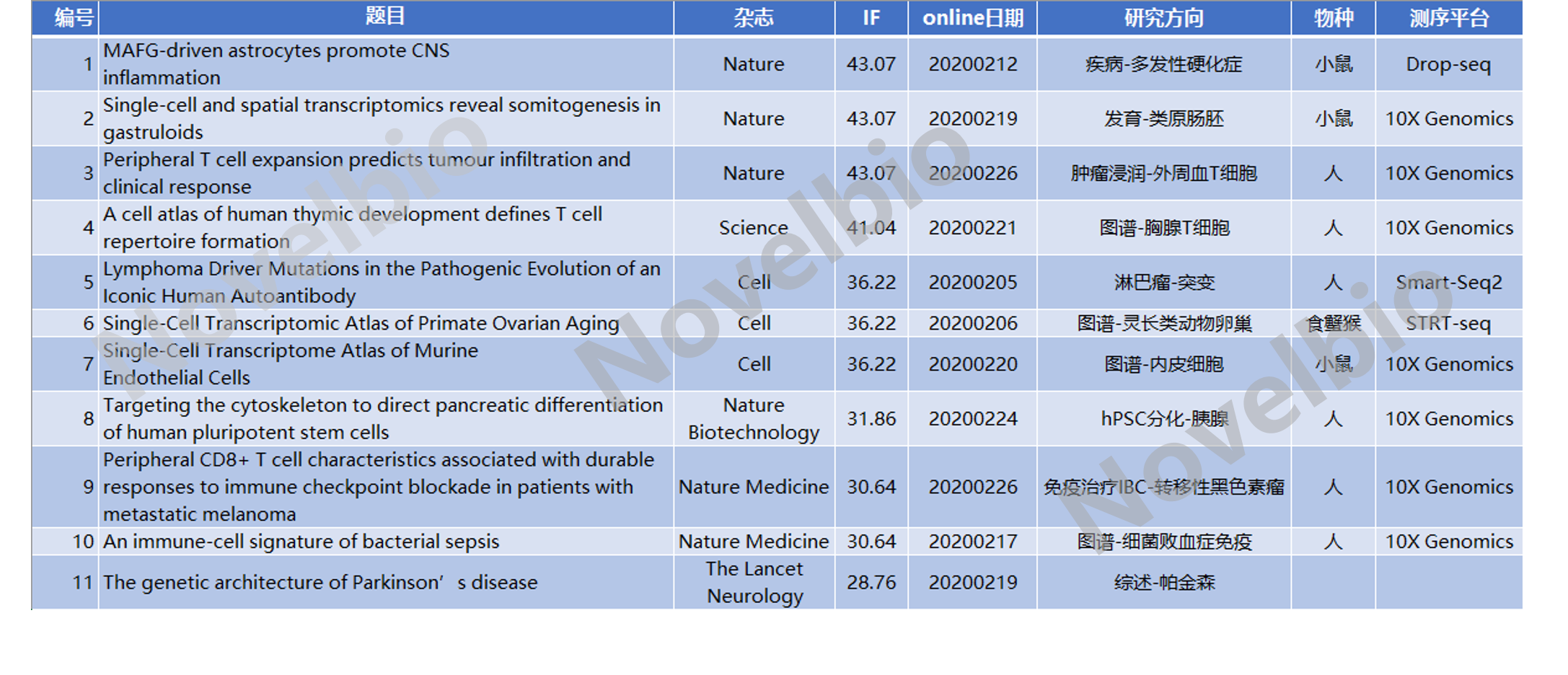
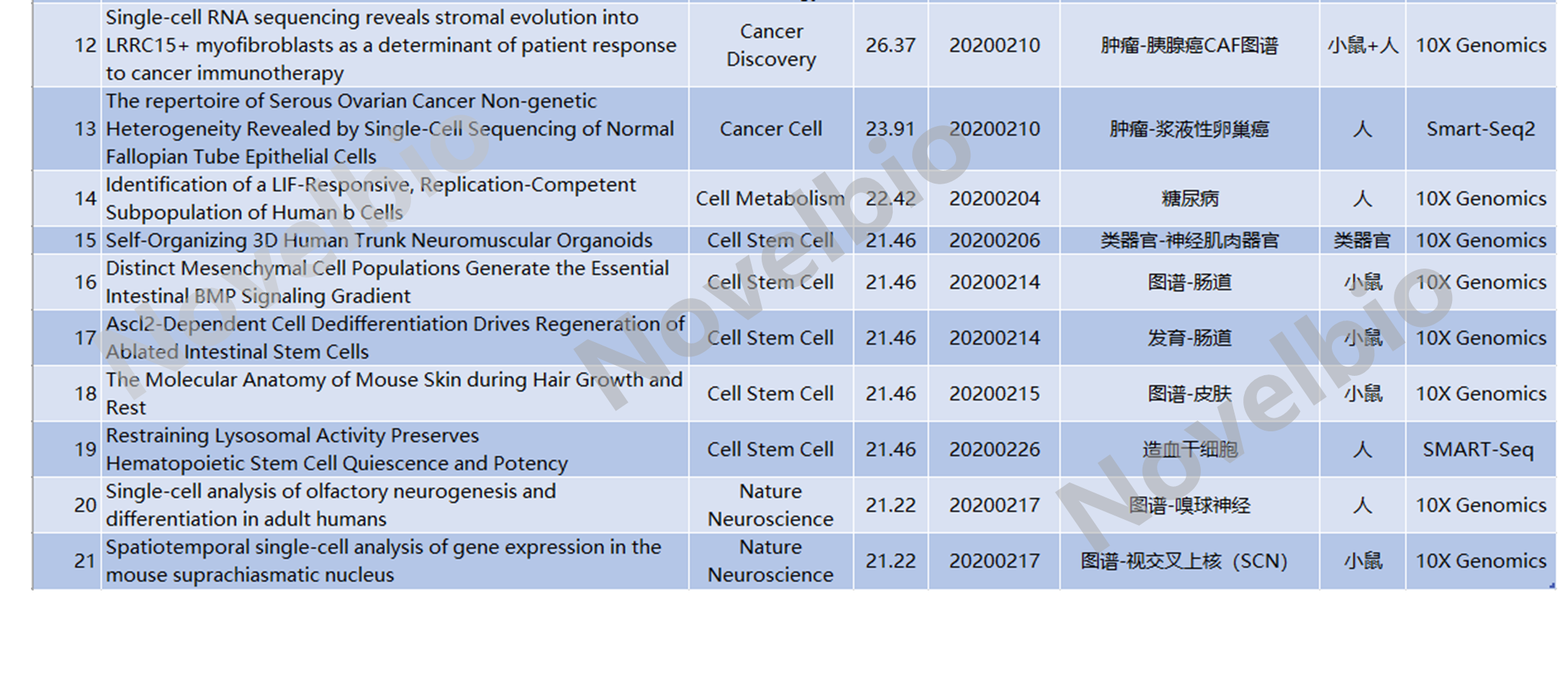
更多scRNA-Seq高分文献汇总如下表:
单细胞转录组测序文献分享
1
单细胞转录组联合TCR||阿尔茨海默氏病人脑脊液中存在克隆扩增的CD8+T细胞
2
Nature||单细胞转录组测序和ATAC-Seq联合解码人类大脑海马体体发育与形成机制
3
单细胞转录组联合空间转录组学||揭示骨髓造血微环境的分子,细胞和空间组织构架

扫描下方二维码,关注“烈冰生物”公众号,获取更多详细信息!