自烈冰生物关键技术——冷冻切片制备亮相以后,很多老师都对烈冰的空间转录组测序保持极大地关注,尤其之前小编请到了实验团队大神Dr.Han亲自上手,结合实际操作详细介绍了样本制备的整个过程,老师们纷纷反馈注意到了很多之前忽略的细节操作。
那么,本期小编就持续高能输出技术干货,介绍一下烈冰生物的数字切片扫描成像方案以及空转实验的核心步骤——组织透化优化,全程高能,做好准备哦~

扫描成像的分辨率是影响组织切片原始图像信息精度和准确度的重要因素。将组织切片扫描为包含所有组织信息的高分辨率电子图片,可以在电脑上进行放大和缩小,如同在显微镜上操作一样,真正将物质的切片标本快速数字化,实现病理数字阅片。
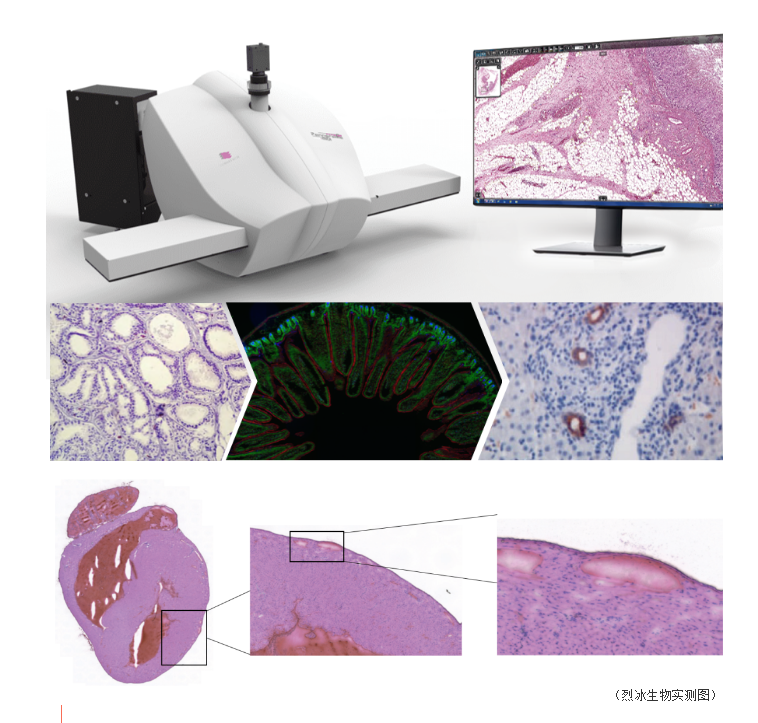

组织透化是指将组织切片放置在含有与 RNA 结合捕获探针的载玻片上,固定染色后,通过透化酶处理的方式,使细胞中的 mRNA 释放并结合到相应的捕获探针上,从而获取基因表达信息。 这个过程需要对透化时间进行一个很好的把控,透化时间不够,mRNA无法充分释放出来;透化时间过长,mRNA可能会扩散到附近区域,影响分析结果的准确性。根据实验人员的操作手法、组织类型、切片厚度等因素不同,最佳透化时间也不尽相同。因此在正式的组织透化实验之前,通常需要对组织进行透化优化,以确定最佳透化时间。
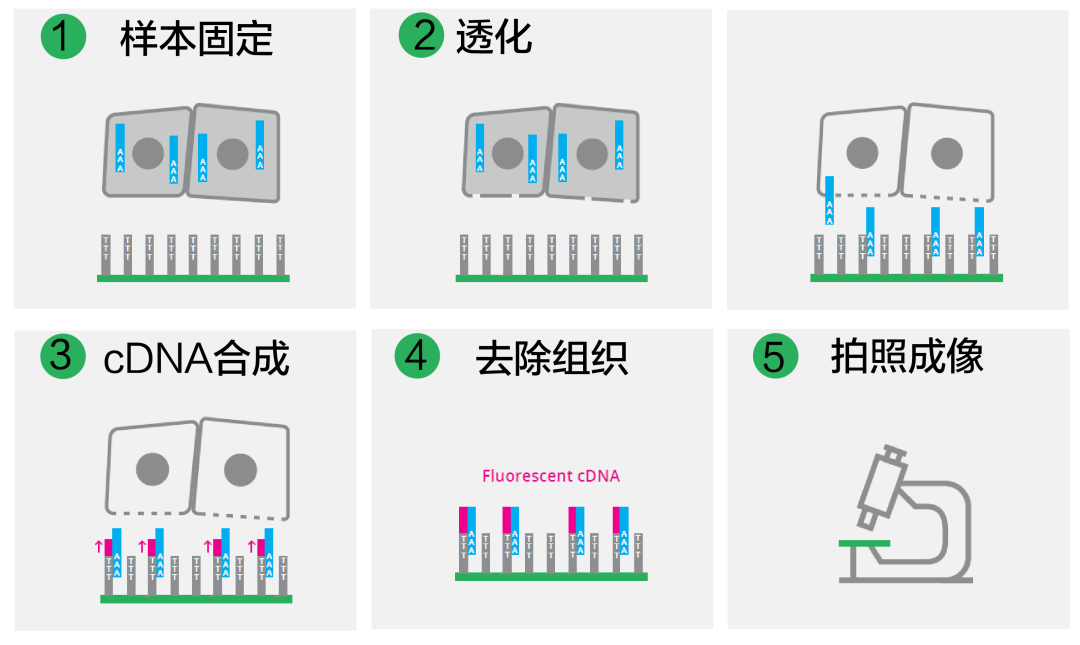
下面就以脑组织的冷冻切片为例详细介绍一下组织透化时间的优化过程。
首先,准备好组织优化的冷冻切片,进行固定、HE染色,然后在明场光源下进行扫描成像。

固定及HE染色具体步骤:
1 )将芯片放在PCR仪上,37°C下孵育1分钟。
2 )将芯片完全浸入预冷的甲醇中在-20°C孵育30分钟。
3 )玻片取出,擦干背面液体,在玻片上滴加500μl异丙醇,室温孵育1分钟;
4 )将芯片上试剂去除,晾干玻片;
5 )加入1 ml苏木精,室温孵育7分钟;
6 )去除苏木精试剂,然后将芯片先浸入无酶水中清洗后,晾干;
7 )加入1 ml Bluing Buffer,室温孵育2分钟;
8 )去除试剂,将芯片浸入无酶水清洗后,擦干玻片背面液体;
9 )加入1 ml伊红混合物,室温孵育1分钟;
10) 去除试剂,将芯片浸入无酶水中清洗,晾干直至组织不透明。
11 )在37°C下孵育芯片5分钟后,进行明场成像实验。
组织透化优化:
组织优化芯片包含8个捕获区域:

组织透化具体步骤:
1)将芯片放在芯片盒中,阳性和阴性对照均不加透化酶。
2 ) 在透化30min的孔中添加70µl透化酶,放置在37°C的PCR适配器上。
3 ) 6分钟后,向透化24min的孔中添加70µl通透酶,并在37°C的PCR适配器上孵育,
4) 重复此过程,直至27min后,向透化3min的孔添加70µl透化酶,放置在37°C的PCR适配器上。
5) 从每个孔中除去透化酶,阳性对照以外的所有孔中添加100µl 0.1X SSC,
6) 从每个孔中移出0.1X SSC。向每个孔中加入50µl Fluorescent RT Master Mix,将其放在预热的PCR仪(设置条件)以启动cDNA合成。
7) 从孔中吸出Fluorescent RT Master Mix,向每个孔中添加100µl 0.1X SSC,
8) 从每个孔中吸出0.1X SSC。向每个孔中加入70µl Tissue Removal Mix,然后放在PCR仪适配器上孵育,
9) 从孔中吸出Tissue Removal Mix。从芯片盒中取出芯片,浸入预热的2X SSC-0.1%SDS中15次,浸入0.2X SSC中15次,浸入0.1X SSC中15次。
10) 在载片旋转器中离心30s,确认芯片上没有剩余的组织。
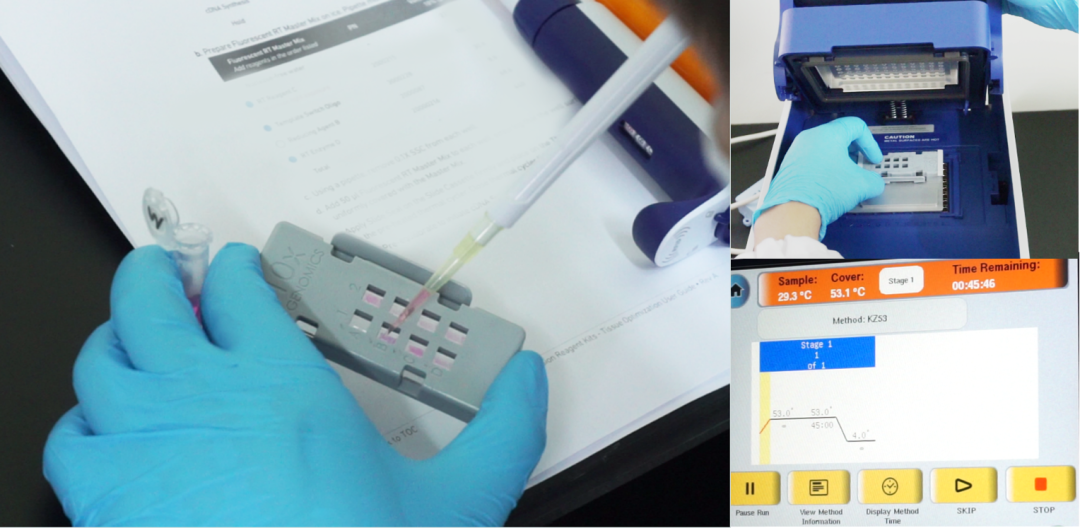
通过数字切片扫描仪在荧光场下进行扫描成像。可以明显看出随着透化时间的延长,荧光强度先逐渐增强,透化12min时荧光亮度达到最亮,而后逐渐减弱。
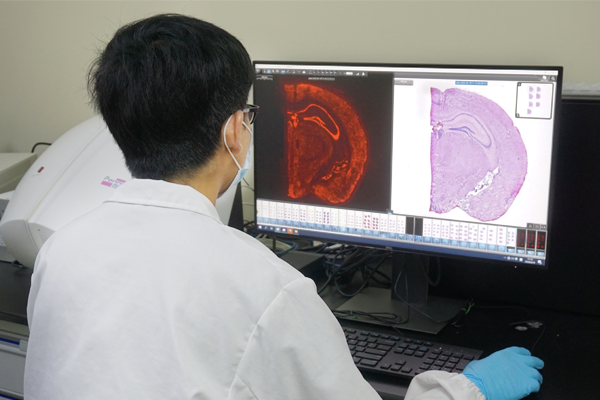
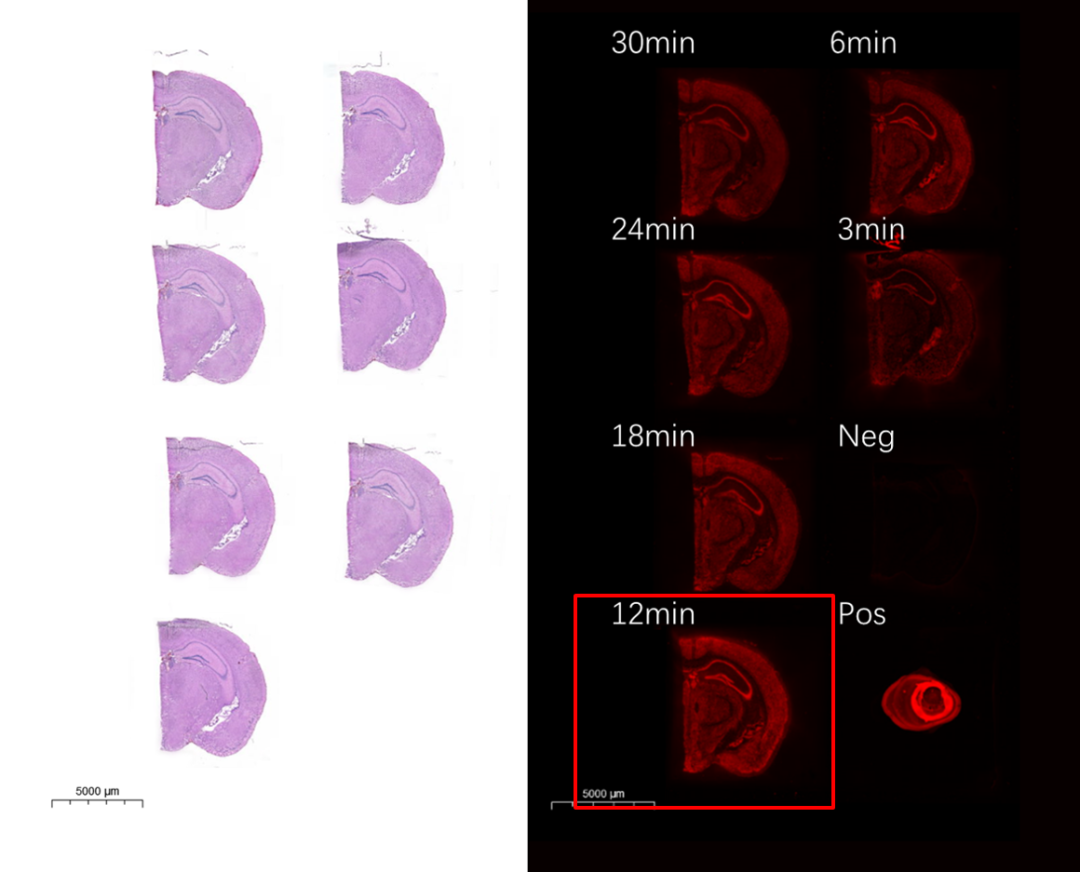
如果荧光强度接近,可以选择较长的透化时间,防止透化不充分。但透化时间并不是越长越好,随着时间增加,细胞内释放的RNA会扩散,进入附近组织区域,放大看到海马区结构模糊,或向边缘扩散,没有荧光信号的区域也出现了荧光信号。所以,在选择最佳透化时间时,应综合考虑荧光强度以及RNA扩散程度。
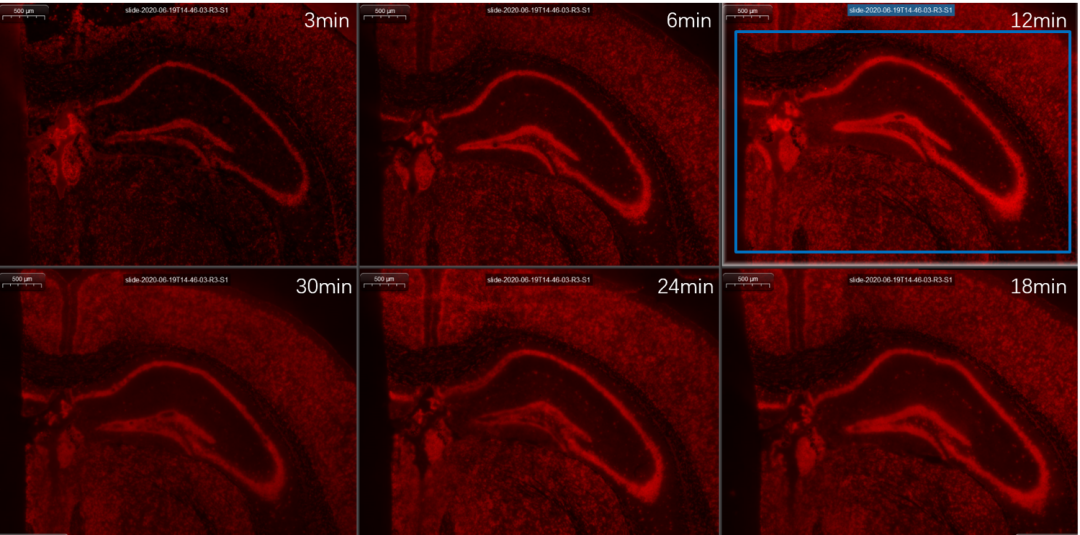
选择最佳的透化时间后,就可以进行正式实验了。正式实验流程与组织透化优化的实验流程基本一致,只是所用芯片不一样。正式实验用的基因表达芯片上有4个捕获区域,其实验流程为:
冷冻切片及贴片→甲醇固定→HE染色→明场拍照→透化→cDNA合成→第二链cDNA合成→变性→cDNA扩增→纯化和质控→片段化,末端修复,加A→连接头→样本index PCR→上机测序。

热点回顾:
